spectrumnews.org Traduction de "Antihistamine aids myelination in Pitt-Hopkins mice" par Laura Dattaro - 25 mai 2023

Agrandissement : Illustration 1
En juin dernier, Brady Maher a donné une conférence sur les possibilités de reconversion de médicaments existants pour les personnes atteintes du syndrome de Pitt-Hopkins, une maladie génétique rare qui s'accompagne souvent d'autisme. Parmi les composés qu'il a mentionnés figure l'antihistaminique clemastine fumurate, qui est disponible sur ordonnance aux États-Unis, souvent sous le nom de marque Tavist. En plus de soulager les allergies, la clémastine favorise la croissance de la myéline, la couche lipidique qui isole les neurones comme une gaine de plastique autour d'un fil.
Environ un mois plus tard, M. Maher a reçu un courriel d'un parent qui avait écouté sa conférence, prononcée lors d'une réunion de la Pitt Hopkins Research Foundation (PHRF) à Chicago, dans l'Illinois. Aiden, le fils de Geetika Bajpai, alors âgé de 2 ans, est atteint du syndrome de Pitt-Hopkins, et Bajpai voulait essayer la clemastine.
Maher, chercheur principal à l'Institut Lieber pour le développement du cerveau à Baltimore, dans le Maryland, n'était pas sûr : la clemastine n'est pas autorisée pour les jeunes enfants et il n'existe pas de données sur la façon dont les enfants atteints de la maladie de Pitt-Hopkins pourraient y répondre. De plus, Maher est un chercheur, pas un médecin. Il lui a suggéré d'en parler au pédiatre de son fils, qui a accepté de prescrire le médicament pour les allergies d'Aiden - et de voir s'il avait d'autres effets.
À ce jour, la plupart des connaissances sur les capacités de la clemastine à renforcer la myéline proviennent d'études animales. Mais il semble que le médicament améliore les lésions du tissu cérébral chez les personnes atteintes de sclérose en plaques, une maladie dans laquelle le système immunitaire attaque la myéline et les cellules qui la produisent, appelées oligodendrocytes. Par exemple, le médicament améliore la signalisation du nerf optique chez les adultes atteints de cette maladie, selon les résultats d'essais cliniques menés en 2017.
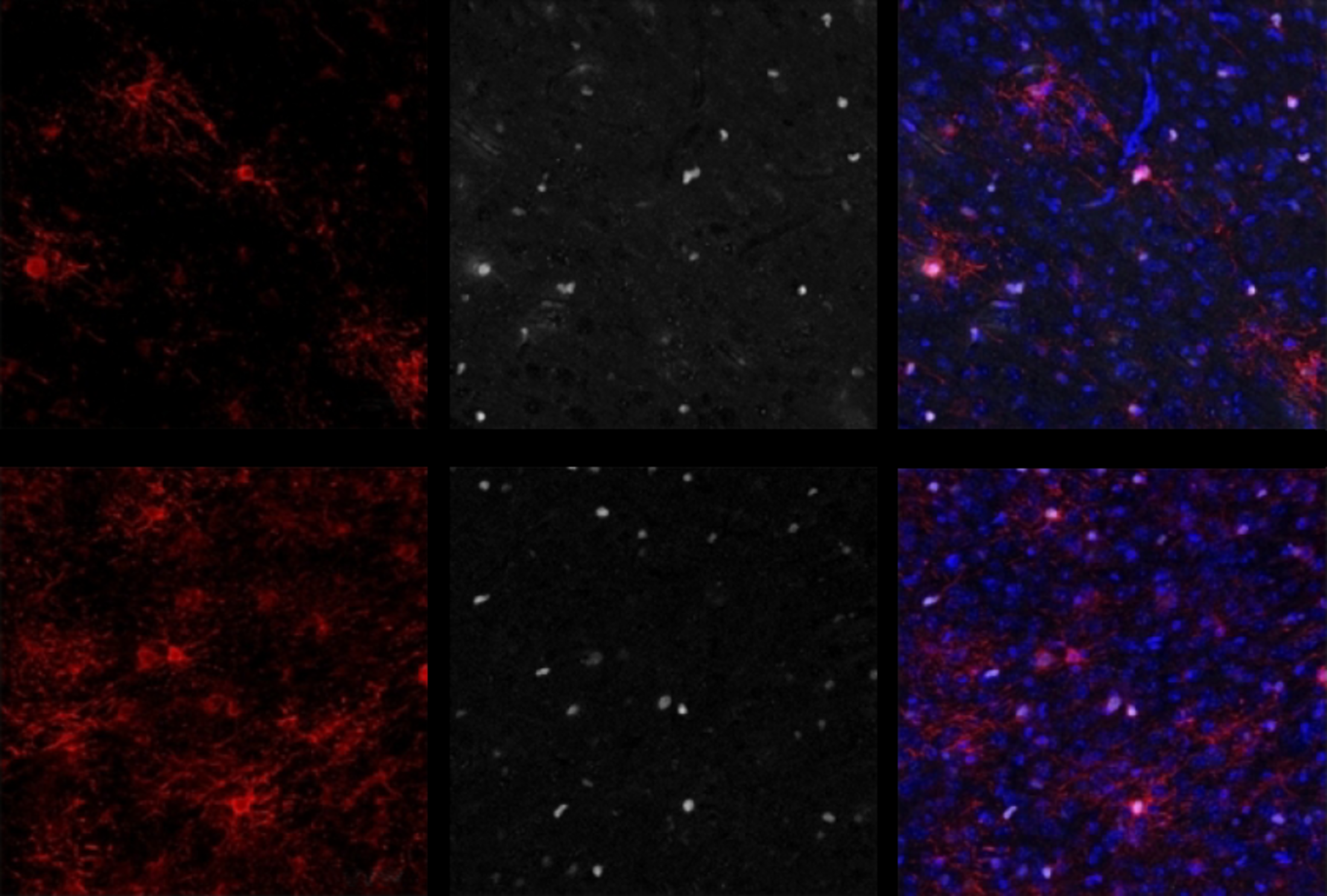
Il est raisonnable de penser que l'augmentation de la myélinisation pourrait également atténuer les caractéristiques de certaines conditions neurodéveloppementales, y compris le syndrome de Pitt-Hopkins : les souris présentant des mutations observées chez les personnes atteintes de cette maladie expriment différemment les gènes des oligodendrocytes et ont moins de cellules et de myéline, a constaté Maher dans une étude de 2020. La clémastine améliore la myélinisation et normalise l'activité cérébrale et le comportement des souris, a-t-il constaté dans une étude publiée dans Brain en avril. Il en va de même pour un composé expérimental appelé sobétirome, qui imite l'hormone thyroïdienne - nécessaire à la myélinisation - et pour une version simplifiée du médicament, appelée Sob-AM2, qui traverse plus facilement la barrière hémato-encéphalique.
Les preuves qui s'accumulent sont suffisantes pour que les chercheurs envisagent un essai clinique de médicaments promyélinisants chez les enfants atteints du syndrome de Pitt-Hopkins, selon Maher. La clemastine et le Sob-AM2 présentent tous deux des avantages et des inconvénients : Il est possible que la clemastine puisse être testée plus rapidement puisqu'elle a déjà été approuvée par la Food and Drug Administration américaine, explique Maher, mais elle aurait probablement plus d'effets secondaires que le Sob-AM 2 ; les antihistaminiques peuvent causer de la somnolence et un ralentissement des facultés cognitives. Les deux médicaments devront probablement faire l'objet de tests de toxicologie chez les nouveau-nés ou les très jeunes animaux.
Selon Kimberly Goodspeed, professeure adjointe de pédiatrie, de neurologie et de psychiatrie à l'UT Southwestern Medical Center de Dallas, au Texas, les données obtenues sur les animaux sont prometteuses mais préliminaires. Goodspeed n'a pas participé aux travaux de Maher mais traite des enfants atteints du syndrome de Pitt-Hopkins.
"Il s'agit d'une découverte passionnante, mais il faudrait peut-être encore une étude sur les souris ou les rats avant de l'appliquer à l'homme", dit-elle. "Il s'agit d'une preuve de concept très intéressante."
Thomas Scanlan a lu l'étude 2020 de Maher avec grand intérêt. Scanlan, professeur de physiologie chimique et de pharmacologie à l'Oregon Health & Science University de Portland, a créé le sobetirome en 1996 pour traiter l'hypercholestérolémie, qui est modérée par l'hormone thyroïdienne. Mais au début des années 2000, alors que les preuves que l'hormone thyroïdienne favorise la remyélinisation s'accumulaient, Scanlan a pivoté pour étudier le médicament dans le système nerveux central et, en 2017, a développé le Sob-AM2.
En 2018, Scanlan a cofondé une société appelée aujourd'hui Autobahn, qui vise à tester le Sob-AM2 et des médicaments similaires chez des personnes atteintes de sclérose en plaques ou de dépression majeure. Le sobétirome et le Sob-AM2 aident les souris dépourvues de myéline à régénérer l'isolation, a-t-il montré en 2019.
Dans la souris Pitt-Hopkins de Maher, Scanlan a vu une autre opportunité pour le Sob-AM2.
Scanlan a envoyé un courriel à Maher quelques semaines après la publication de l'article de 2020, alors que Maher étudiait déjà l'utilisation de la clemastine et d'autres médicaments promyélinisants chez les souris Pitt-Hopkins. Maher a accepté d'essayer les médicaments de Scanlan sur ses animaux. Comme l'équipe l'a décrit dans Brain en avril, les cultures cellulaires des souris Pitt-Hopkins avaient moins d'oligodendrocytes et plus de précurseurs d'oligodendrocytes que les souris de type sauvage, et le fait de baigner les cultures dans la clemastine a réduit cette différence. Les tranches de cerveau d'animaux ayant reçu des injections de clémastine dans l'estomac ont montré la même chose, et les effets ont duré près de sept semaines après la fin du traitement de deux semaines.
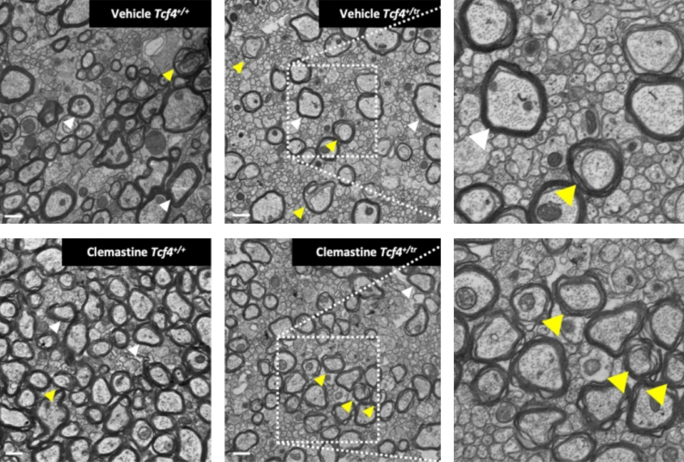
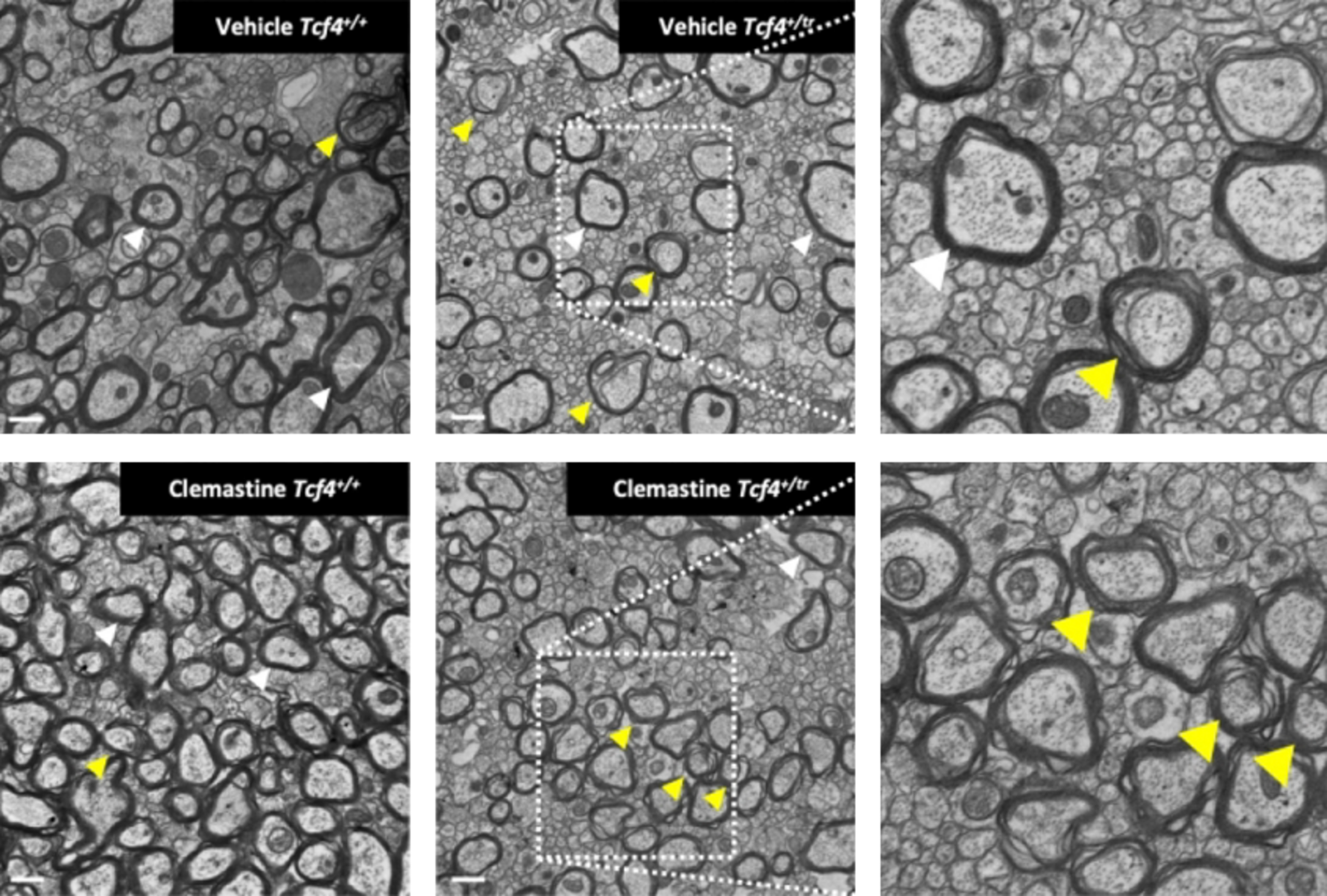
Les axones des tranches de souris Pitt-Hopkins traitées présentaient des signes de myélinisation plus importante que ceux des souris non traitées - à peu près autant que les souris de type sauvage, ont constaté les chercheurs à l'aide de la microscopie électronique à transmission. Les enregistrements par électrodes ont révélé que les souris traitées présentent un rapport plus typique entre les signaux voyageant le long des axones myélinisés et non myélinisés que les souris non traitées. (Maher n'a pas testé ce rapport chez les témoins).
Les souris modèles non traitées se sont également comportées de manière inhabituelle dans un espace ouvert : elles gambadent beaucoup plus que les souris sauvages et se déplacent fréquemment vers le centre de l'espace, ce qui témoigne d'un manque d'anxiété atypique. Ces deux comportements se sont normalisés avec le traitement à la clemastine. L'administration de Sob-AM2 a eu les mêmes effets, et le sobetirome a rétabli les niveaux d'oligodendrocytes et de précurseurs d'oligodendrocytes de type sauvage chez les animaux.
Toute personne souhaitant tester le Sob-AM2 chez l'homme devra obtenir une licence de l'Oregon Health & Science University, qui détient le brevet. (Le brevet sur le sobetirome a expiré en 2016, mais le médicament ne serait pas un bon candidat clinique pour les affections cérébrales en raison de sa difficulté à traverser la barrière hémato-encéphalique, explique M. Scanlan). Il devrait également soumettre une demande de nouveau médicament expérimental à la Food and Drug Administration.
L'innocuité du médicament n'a jamais été testée chez l'homme et il n'existe aucune donnée sur les doses à utiliser. "C'est une possibilité à laquelle on peut penser à l'avenir", déclare M. Scanlan. "Mais ce n'est pas pour demain. (Autobahn ne prévoit pas pour l'instant d'étudier le Sob-AM2 dans le syndrome de Pitt-Hopkins, précise Scanlan).
La clemastine, en revanche, pourrait faire l'objet d'un essai académique dès maintenant. Un tel essai pourrait fournir une nouvelle "preuve de concept" pour l'utilisation de médicaments myélinisants dans le traitement de la maladie de Pitt-Hopkins, explique Scanlan, bien que les effets secondaires sédatifs de la clemastine et son absorption cérébrale limitée ne la rendent pas idéale pour une utilisation régulière. "Ni l'un ni l'autre n'est tout à fait prêt à entrer en phase de développement clinique."
Agrandissement : Illustration 2
Malgré cela, les familles dont les enfants sont atteints de la maladie peuvent être désireuses de participer à un essai. Environ 1 100 personnes dans le monde sont atteintes du syndrome de Pitt-Hopkins, selon un recensement géré par la PHRF. Et les parents sont souvent disposés à essayer de nouveaux traitements, selon Goodspeed. Après que M. Maher a testé un composé expérimental sur des souris atteintes du syndrome de Pitt-Hopkins en 2016, par exemple, PHRF a présenté l'étude comme un "traitement potentiel". Et plusieurs familles ont voulu essayer la nicardipine, un médicament contre la tension artérielle, à la suite d'une étude réalisée en 2020 montrant que ce médicament améliorait les comportements sociaux et répétitifs chez des souris modèles, explique Mme Goodspeed.
Les enfants qui ont déjà essayé la clemastine seraient probablement exclus de tout essai, dit Maher. Mais il y a 406 enfants connus pour être atteints de la maladie de Pitt-Hopkins aux États-Unis et, à la connaissance de Maher, seuls 3 ont pris de la clemastine.
Les deux médicaments devront probablement faire l'objet de tests de toxicologie chez les nouveau-nés ou les très jeunes animaux.
Selon Kimberly Goodspeed, professeure adjointe de pédiatrie, de neurologie et de psychiatrie à l'UT Southwestern Medical Center de Dallas, au Texas, les données obtenues sur les animaux sont prometteuses mais préliminaires. Goodspeed n'a pas participé aux travaux de Maher mais traite des enfants atteints du syndrome de Pitt-Hopkins.
"Il s'agit d'une découverte passionnante, mais il faudrait peut-être encore une étude sur les souris ou les rats avant de l'appliquer à l'homme", dit-elle. "Il s'agit d'une preuve de concept très intéressante."
Thomas Scanlan a lu l'étude 2020 de Maher avec grand intérêt. Scanlan, professeur de physiologie chimique et de pharmacologie à l'Oregon Health & Science University de Portland, a créé le sobetirome en 1996 pour traiter l'hypercholestérolémie, qui est modérée par l'hormone thyroïdienne. Mais au début des années 2000, alors que les preuves que l'hormone thyroïdienne favorise la remyélinisation s'accumulaient, Scanlan a pivoté pour étudier le médicament dans le système nerveux central et, en 2017, a développé le Sob-AM2.
En 2018, Scanlan a cofondé une société appelée aujourd'hui Autobahn, qui vise à tester le Sob-AM2 et des médicaments similaires chez des personnes atteintes de sclérose en plaques ou de dépression majeure. Le sobétirome et le Sob-AM2 aident les souris dépourvues de myéline à régénérer l'isolation, a-t-il montré en 2019.
Dans la souris Pitt-Hopkins de Maher, Scanlan a vu une autre opportunité pour le Sob-AM2.
Scanlan a envoyé un courriel à Maher quelques semaines après la publication de l'article de 2020, alors que Maher étudiait déjà l'utilisation de la clemastine et d'autres médicaments promyélinisants chez les souris Pitt-Hopkins. Maher a accepté d'essayer les médicaments de Scanlan sur ses animaux. Comme l'équipe l'a décrit dans Brain en avril, les cultures cellulaires des souris Pitt-Hopkins avaient moins d'oligodendrocytes et plus de précurseurs d'oligodendrocytes que les souris de type sauvage, et le fait de baigner les cultures dans la clemastine a réduit cette différence. Les tranches de cerveau d'animaux ayant reçu des injections de clémastine dans l'estomac ont montré la même chose, et les effets ont duré près de sept semaines après la fin du traitement de deux semaines.
Les axones des tranches de souris Pitt-Hopkins traitées présentaient des signes de myélinisation plus importante que ceux des souris non traitées - à peu près autant que les souris de type sauvage, ont constaté les chercheurs à l'aide de la microscopie électronique à transmission. Les enregistrements par électrodes ont révélé que les souris traitées présentent un rapport plus typique entre les signaux voyageant le long des axones myélinisés et non myélinisés que les souris non traitées. (Maher n'a pas testé ce rapport chez les témoins).
Les souris modèles non traitées se sont également comportées de manière inhabituelle dans un espace ouvert : elles gambadent beaucoup plus que les souris sauvages et se déplacent fréquemment vers le centre de l'espace, ce qui témoigne d'un manque d'anxiété atypique. Ces deux comportements se sont normalisés avec le traitement à la clemastine. L'administration de Sob-AM2 a eu les mêmes effets, et le sobetirome a rétabli les niveaux d'oligodendrocytes et de précurseurs d'oligodendrocytes de type sauvage chez les animaux.
Toute personne souhaitant tester le Sob-AM2 chez l'homme devra obtenir une licence de l'Oregon Health & Science University, qui détient le brevet. (Le brevet sur le sobetirome a expiré en 2016, mais le médicament ne serait pas un bon candidat clinique pour les affections cérébrales en raison de sa difficulté à traverser la barrière hémato-encéphalique, explique M. Scanlan). Il devrait également soumettre une demande de nouveau médicament expérimental à la Food and Drug Administration.
L'innocuité du médicament n'a jamais été testée chez l'homme et il n'existe aucune donnée sur les doses à utiliser. "C'est une possibilité à laquelle on peut penser à l'avenir", déclare M. Scanlan. "Mais ce n'est pas pour demain. (Autobahn ne prévoit pas pour l'instant d'étudier le Sob-AM2 dans le syndrome de Pitt-Hopkins, précise Scanlan).
La clemastine, en revanche, pourrait faire l'objet d'un essai académique dès maintenant. Un tel essai pourrait fournir une nouvelle "preuve de concept" pour l'utilisation de médicaments myélinisants dans le traitement de la maladie de Pitt-Hopkins, explique Scanlan, bien que les effets secondaires sédatifs de la clemastine et son absorption cérébrale limitée ne la rendent pas idéale pour une utilisation régulière. "Ni l'un ni l'autre n'est tout à fait prêt à entrer en phase de développement clinique."
Aide à l'axone : Après l'injection de clémastine, les axones des souris Pitt-Hopkins ont plus de myéline (flèches jaunes et blanches) que les souris qui n'ont pas reçu le médicament.
Malgré cela, les familles dont les enfants sont atteints de la maladie peuvent être désireuses de participer à un essai. Environ 1 100 personnes dans le monde sont atteintes du syndrome de Pitt-Hopkins, selon un recensement géré par la PHRF. Et les parents sont souvent disposés à essayer de nouveaux traitements, selon Goodspeed. Après que M. Maher a testé un composé expérimental sur des souris atteintes du syndrome de Pitt-Hopkins en 2016, par exemple, PHRF a présenté l'étude comme un "traitement potentiel". Et plusieurs familles ont voulu essayer la nicardipine, un médicament contre la tension artérielle, à la suite d'une étude réalisée en 2020 montrant que ce médicament améliorait les comportements sociaux et répétitifs chez des souris modèles, explique Mme Goodspeed.
Les enfants qui ont déjà essayé la clemastine seraient probablement exclus de tout essai, dit Maher. Mais il y a 406 enfants connus pour être atteints de la maladie de Pitt-Hopkins aux États-Unis et, à la connaissance de Maher, seuls 3 ont pris de la clemastine.



